Teràpia en Distròfia Muscular de Duchenne
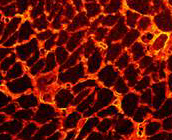 Es tracta d’un estudi intervencional terapèutic en un model preclínic de distròfia muscular de Duchenne. Hem realitzat un estudi amb Nintedanib, un fàrmac amb una activitat antitirosina-cinasa en un model murí mdx de distròfia muscular de Duchenne. Nintedanib és un fàrmac que bloqueja els receptors de PDGF-AA, PDGF-BB, VEGF i bFGF. Aquest tractament ha estat aprovat recentment per la fibrosis pulmonar idiopàtica i està en fase d’assaig en esclerodèrmia. Nosaltres hem decidit utilitzar-lo en models de distròfia muscular per la evidència recent de que PDFG-AA és un factor associat al procés de fibrosis muscular. De fet, gràcies a aquest estudi hem pogut identificar que PDGF-AA és un factor clau en la proliferació i quimiotaxis dels fibroblasts obtinguts de biòpsies musculars in vitro. PDGF-AA estimula l’expressió de col·làgen I per part d’aquestes cèl·lules in vitro. B-FGF és clau en la proliferació de mioblasts o miotubs.
Es tracta d’un estudi intervencional terapèutic en un model preclínic de distròfia muscular de Duchenne. Hem realitzat un estudi amb Nintedanib, un fàrmac amb una activitat antitirosina-cinasa en un model murí mdx de distròfia muscular de Duchenne. Nintedanib és un fàrmac que bloqueja els receptors de PDGF-AA, PDGF-BB, VEGF i bFGF. Aquest tractament ha estat aprovat recentment per la fibrosis pulmonar idiopàtica i està en fase d’assaig en esclerodèrmia. Nosaltres hem decidit utilitzar-lo en models de distròfia muscular per la evidència recent de que PDFG-AA és un factor associat al procés de fibrosis muscular. De fet, gràcies a aquest estudi hem pogut identificar que PDGF-AA és un factor clau en la proliferació i quimiotaxis dels fibroblasts obtinguts de biòpsies musculars in vitro. PDGF-AA estimula l’expressió de col·làgen I per part d’aquestes cèl·lules in vitro. B-FGF és clau en la proliferació de mioblasts o miotubs.
A una segona fase, hem vist com Nintedanib redueix la proliferació i quimiotaxis dels fibroblasts in vitro. Aquest fàrmac produeix canvis en l’expressió gènica dels fibroblasts en cultiu. S’ha determinat una clara reducció en l’expressió de col·làgen I i III i de fibronectina in vitro. A més, el fàrmac produeix una reducció de l’expressió de factors de creixement profibròtics per part dels fibroblasts, com són PDGF-AA, CTGF o TGF-beta.
Finalment, hem tractat un grup de ratolins mdx amb Nintedanib durant 4 setmanes. Hem detectat una millora funcional en l’amplitud dels potencials motors evocats utilitzant tècniques d’electromiografia. Els estudis histològics han demostrat una reducció dels infiltrats inflamatoris i un descens de l’àrea de teixit fibròtic present a les biòpsies. Els estudis d’expressió gènica han mostrat una reducció en l’expressió dels gens de col·lagen I i III i dels factors de creixement probibròtic PDGF-AA, TGF-beta i CTGF. Aquests resultats s’han confirmat mitjançant WB mostrant reducció de les proteïnes codificades per aquests gens.
teràpia en disferlinopaties
La disferlina és una proteïna transmembrana implicada en la reparació del sarcolema de les fibres musculars. Les disferlinopaties estan causades per mutacions en el gen DYSF i poden causar un grup heterogeni de malalties autosòmiques recessives, com la distròfia muscular de cintures 2B (és la segona distròfia de cintures més freqüent a Espanya), la miopatia de Miyoshi i la miopatia distal del compartiment anterior. Encara no s’ha trobat un tractament efectiu per a aquesta malaltia.
Les proteïnes generades pels gens mutats són reconegudes per la cèl·lula com anòmales i són destruïdes per uns mecanismes concrets (proteasoma).
No obstant això, algunes d’aquestes mutacions donen lloc a proteïnes que, encara que són anòmales, conserven part de la seva funció però que són degradades igualment. Els nostres estudis pretenen demostrar que si aconseguim evitar la destrucció de les proteïnes que conserven una mica de funció podríem observar una millora a llarg termini dels símptomes clínics.
En les biòpsies musculars d’aquests pacients s’ha descrit la presència d’inflamació, principalment de cèl·lules T CD4 + i macròfags. A més, l’absència de disferlina produeix una reparació de membrana deficient que pot resultar en l’alliberament de alarmines endògenes produint-se un augment de l’assenyalament via TLR4, receptor que las seva expressió pot estar incrementada en el múscul esquelètic d’aquests pacients. El nostre estudi està destinat a disminuir la senyalització de l’inflamasoma en pacients amb disferlinopatía. Per a això s’estudiaran potencials lligands de TLR4, així com l’expressió de missatgers secundaris en cèl·lules deficients en disferlina que activarien la immunitat innata. L’estudi i identificació dels components de la via de senyalització implicada en la resposta inflamatòria observada en les disferlinopaties, ens permetrà avaluar l’eficàcia de diferents tractaments farmacològics, destinats a disminuir la inflamació. També avaluarem altres fàrmacs destinats a incrementar l’expressió de disferlina.