Terapia en Distrofia Muscular de Duchenne
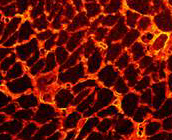 Se trata de un estudio intervencional terapéutico en un modelo preclínico de distrofia muscular de Duchenne. Hemos realizado un estudio con nintedanib, un fármaco con actividad antitirosin-quinasa en un modelo murino mdx de distrofia muscular de Duchenne. Nintedanib es un fármaco que bloquea los receptores de PDGF-AA, PDGF-BB, VEGF y bFGF. Este tratamiento ha sido aprobado recientemente para la fibrosis pulmonar idiopática y está en fase de ensayo en la esclerodermia. Nosotros hemos decidido utilizarlo en modelos de distrofia muscular por la evidencia reciente de que PDGF-AA es un factor asociado al proceso de fibrosis muscular. De hecho, gracias a este estudio hemos podido identificar que PDGF-AA es un factor clave en la proliferación y quemotaxis de los fibroblastos obtenidos de biopsias musculares in vitro. PDGF-AA estimula la expresión de colágeno I por parte de estas células in vitro. b-FGF es clave en la proliferación de mioblastos in vitro. Ninguno de estos factores interfiere en la diferenciación de los mioblastos a miotubos.
Se trata de un estudio intervencional terapéutico en un modelo preclínico de distrofia muscular de Duchenne. Hemos realizado un estudio con nintedanib, un fármaco con actividad antitirosin-quinasa en un modelo murino mdx de distrofia muscular de Duchenne. Nintedanib es un fármaco que bloquea los receptores de PDGF-AA, PDGF-BB, VEGF y bFGF. Este tratamiento ha sido aprobado recientemente para la fibrosis pulmonar idiopática y está en fase de ensayo en la esclerodermia. Nosotros hemos decidido utilizarlo en modelos de distrofia muscular por la evidencia reciente de que PDGF-AA es un factor asociado al proceso de fibrosis muscular. De hecho, gracias a este estudio hemos podido identificar que PDGF-AA es un factor clave en la proliferación y quemotaxis de los fibroblastos obtenidos de biopsias musculares in vitro. PDGF-AA estimula la expresión de colágeno I por parte de estas células in vitro. b-FGF es clave en la proliferación de mioblastos in vitro. Ninguno de estos factores interfiere en la diferenciación de los mioblastos a miotubos.
En una segunda fase, hemos visto como nintedanib reduce la proliferación y quemotaxis de los fibroblastos in vitro. Este fármaco produce cambios en la expresión génica de los fibroblastos en cultivo. Se ha determinado una clara reducción en la expresión de colágeno I y III y de fibronectina in vitro. Además, el fármaco produce una reducción de la expresión de factores de crecimiento profibróticos por parte de los fibroblastos, como son PDGF-AA, CTGF o TGF-beta.
Finalmente, hemos tratado un grupo de ratones mdx con nintedanib por 4 semanas. Hemos detectado una mejoría funcional en la amplitud de los potenciales motores evocados utilizando técnicas de electromiografía. Los estudios histológicos han demostrado una reducción de los infiltrados inflamatorios y de un descenso del área de tejido fibrótico presente en las biopsias. Los estudios de expresión génica han mostrado una reducción en la expresión de los genes de colágeno I y III y de los factores de crecimiento profibrótico PDGF-AA, TGF-beta y CTGF. Estos resultados se han confirmado mediante WB mostrando reducción de las proteínas codificadas por estos genes.
TERAPIA EN DISFERLINOPATÍAS
La disferlina es una proteína transmembrana implicada en la reparación del sarcolema de las fibras musculares. Las disferlinopatías están causadas por mutaciones en el gen DYSF y pueden causar un grupo heterogéneo de enfermedades autosómicas recesivas, como la distrofia muscular de cinturas 2B (es la segunda distrofia de cinturas más frecuente en España), la miopatía de Miyoshi y la miopatía distal del compartimento anterior. Todavía no se ha encontrado un tratamiento efectivo para esta enfermedad.
Las proteínas generadas por los genes mutados son reconocidas por la célula como anómalas y son destruídas por unos mecanismos concretos (proteasoma).
Sin embargo, algunas de estas mutaciones dan lugar a proteínas que, aunque son anómalas, conservan parte de su función pero que son degradadas igualmente. Nuestros estudios pretenden demostrar que si conseguimos evitar la destrucción de las proteínas que conservan algo de función podríamos observar una mejora a largo plazo de los síntomas clínicos.
En las biopsias musculares de éstos pacientes se ha descrito la presencia de inflamación, principalmente de células T CD4+ y macrófagos. Además, la ausencia de disferlina produce una reparación de membrana deficiente que puede resultar en la liberación de alarminas endógenas produciéndose un aumento de la señalación vía TLR4, receptor cuya expresión puede estar incrementada en el músculo esquelético de estos pacientes. Nuestro estudio está destinado a disminuir la señalización del inflamasoma en pacientes con disferlinopatía. Para ello se estudiaran potenciales ligandos de TLR4, así como la expresión de mensajeros secundarios en células deficientes en disferlina que activarían la inmunidad innata. El estudio e identificación de los componentes de la vía de señalización implicada en la respuesta inflamatoria observada en las disferlinopatías, nos permitirá evaluar la eficacia de diferentes tratamientos farmacológicos, destinados a disminuir la inflamación. También evaluaremos otros fármacos destinados a incrementar la expresión de disferlina.